Химия ЕГЭ - банк заданий - страница 54
Вопросы
Установите соответствие между реагирующими веществами и признаком протекающей между ними реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
Установите соответствие между областью применения и веществом: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
К 135 г раствора с массовой долей соли 22 % добавили 25 г этой же соли. Вычислите массовую долю соли в полученном растворе. (Запишите число с точностью до десятых.)
В реакцию, термохимическое уравнение которой
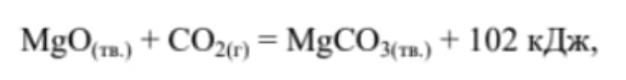
вступило 8,8 г углекислого газа. Какое количество теплоты выделилось при этом? (Запишите число с точностью до десятых.)
Какой объём (н.у.) ацетилена теоретически может быть получен из 235,8 л (н.у.) природного газа, объёмная доля метана в котором равна 95 %? (Запишите число с точностью до целых.)
Для выполнения заданий 1–3 используйте следующий ряд химических элементов:
1) N 2) Al 3) As 4) Cl 5) S
Ответом в заданиях 1–3 является последовательность цифр, под которыми указаны химические элементы в данном ряду.
Определите два элемента, анионы которых содержат такое же число p-электронов, что и катион кальция.
Запишите номера выбранных элементов.
Из указанных в ряду химических элементов выберите три элемента, которые в Периодической системе химических элементов Д.И. Менделеева находятся в одном периоде.
Расположите выбранные элементы в порядке увеличения электроотрицательности их атомов.
Запишите номера выбранных элементов в нужной последовательности.
Из числа указанных в ряду элементов выберите два элемента, которые в соединении с литием проявляют одинаковую степень окисления.
Запишите номера выбранных элементов.
Из предложенного перечня выберите два вещества с немолекулярной кристаллической решёткой, которые имеют ковалентную неполярную химическую связь.
Запишите номера выбранных ответов.
Среди предложенных формул/названий веществ, расположенных в пронумерованных ячейках, выберите формулы/названия: А) соли сернистой кислоты; Б) щёлочи; В) амфотерного оксида.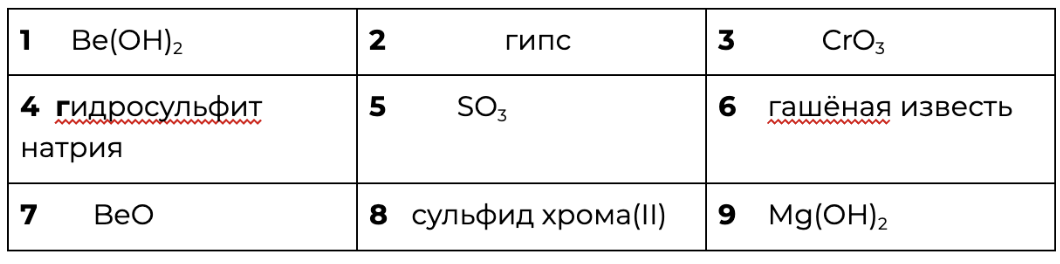
Запишите в таблицу номера ячеек, в которых расположены выбранные вещества, под соответствующими буквами.
