Химия ЕГЭ - банк заданий - страница 51
Вопросы
Для выполнения задания 21 используйте следующие справочные данные.
Концентрация (молярная, моль/л) показывает отношение количества растворённого вещества (n) к объёму раствора (V).
pH («пэ аш») – водородный показатель; величина, которая отражает
концентрацию ионов водорода в растворе и используется для характеристики кислотности среды.
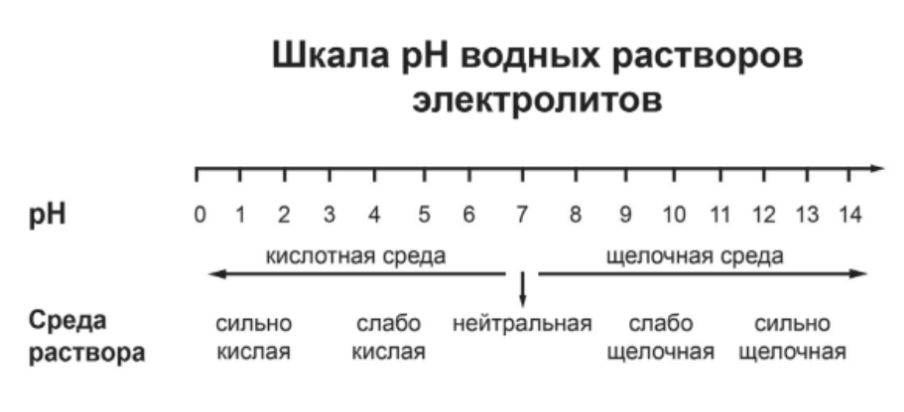
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) Na3PO4
2) CuCl2
3) NaNO3
4) HClO4
Запишите номера веществ в порядке возрастания значения pH их водных растворов, учитывая, что концентрация веществ во всех растворах (моль/л) одинаковая.
Установите соответствие между способом воздействия на равновесную систему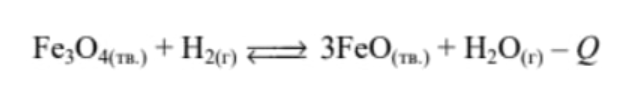
и направлением смещения химического равновесия в результате этого воздействия: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
В реактор постоянного объёма поместили некоторое количество оксида азота(IV) и хлора. В результате протекания обратимой реакции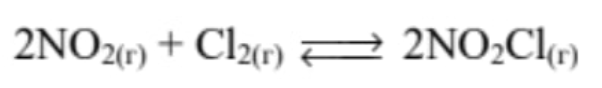
в реакционной системе установилось химическое равновесие, при котором концентрации оксида азота(IV), хлора и хлорида нитроила составили 0,04 моль/л, 0,08 моль/л и 0,16 моль/л соответственно. Определите исходные концентрации NO2 (X) и Cl2 (Y).
Выберите из списка номера правильных ответов:
1) 0,20 моль/л
2) 0,40 моль/л
3) 0,60 моль/л
4) 0,80 моль/л
5) 0,12 моль/л
6) 0,16 моль/л
Запишите выбранные номера в таблицу под соответствующими буквами.
Установите соответствие между реагирующими веществами и признаком протекающей между ними реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
Установите соответствие между полимером и мономером, из которого получают данный полимер: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
К 220 г раствора с массовой долей гидроксида натрия 20 % добавили 44 г воды и 36 г той же щёлочи. Вычислите массовую долю гидроксида натрия в полученном растворе. (Запишите число с точностью до десятых.)
В результате реакции, термохимическое уравнение которой
2CH3Cl(г) + 2Na(тв.) = C2H6(г) + 2NaCl(тв.) + 763 кДж,
образовалось 150 г этана. Определите количество теплоты, которое выделилось при этом. (Запишите число с точностью до целых.)
Вычислите массу (кг) железа, которую можно получить при восстановлении угарным газом образца оксида железа(III) массой 215 кг, если в указанном образце содержится 7 % примеси оксида меди(II). (Запишите число с точностью до целых.)
Для выполнения заданий 1–3 используйте следующий ряд химических элементов:
1) H 2) O 3) Mg 4) V 5) F
Ответом в заданиях 1–3 является последовательность цифр, под которыми
указаны химические элементы в данном ряду.
Определите, атомы каких двух из указанных в ряду элементов в основном состоянии содержат во внешнем электронном слое одинаковое число электронов.
Запишите номера выбранных элементов.
Из указанных в ряду химических элементов выберите три элемента-неметалла.
Расположите выбранные элементы в порядке уменьшения окислительных свойств соответствующих им простых веществ.
Запишите номера выбранных элементов в нужной последовательности.
