Химия ЕГЭ - банк заданий - страница 5
Вопросы
Восстановление оксида железа(III) протекает в соответствии
с термохимическим уравнением реакции
Fe2O3(тв.) + 3H2(г) = 2Fe(тв.) + 3H2O(г) – 89,6 кДж.
Вычислите количество теплоты, которое поглотилось при восстановлении 10 моль оксида железа(III). (Запишите число с точностью до целых.)
Для выполнения задания 1-3 используйте следующий ряд химических элементов:
1) Cs 2) C 3) O 4) Cr 5) N
Ответом в заданиях 1-3 является последовательность цифр, под которыми указаны химические элементы в данном ряду.
Определите, атомы каких из указанных в ряду элементов в основном состоянии имеют одинаковое количество неспаренных электронов.
Запишите номера выбранных элементов.
Из указанных в ряду химических элементов выберите три p-элемента.
Расположите выбранные элементы в порядке уменьшения их атомного радиуса.
Запишите номера выбранных элементов в нужной последовательности.
Из числа указанных в ряду элементов выберите два элемента, которые имеют одинаковую разность между значениями их высшей и низшей степеней окисления.
Запишите номера выбранных элементов.
Установите соответствие между реагирующими веществами и углеродсодержащим продуктом, который образуется при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
Задана схема превращений веществ:
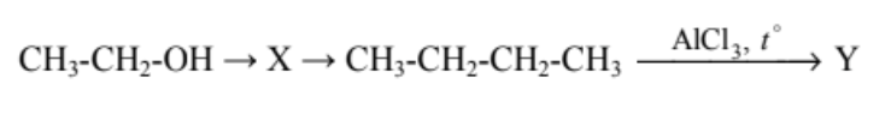
Определите, какие из указанных веществ являются веществами Х и Y.
1) 2-хлорбутан
2) этаналь
3) этилен
4) метилпропан
5) бромэтан
Запишите в таблицу номера выбранных веществ под соответствующими буквами.
Установите соответствие между веществом и возможным способом его получения путём электролиза: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
Для выполнения задания 21 используйте следующие справочные данные.
Концентрация (молярная, моль/л) показывает отношение количества растворённого вещества (n) к объёму раствора (V).
pH («пэ аш») — водородный показатель; величина, которая отражает концентрацию ионов водорода в растворе и используется для характеристики кислотности среды.
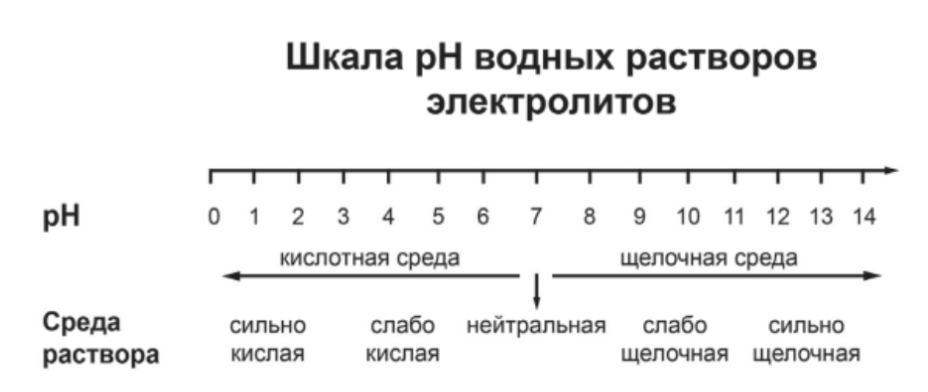
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) Na2SO4
2) Fe(NO3)2
3) K2SO3
4) НClO3
Запишите номера веществ в порядке возрастания значения pH их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая.
Установите соответствие между способом воздействия на равновесную систему
H2O(ж) + Al3+(р-р) ⇄ AlOH2+(р-р) + H+(р-р) – Q
и смещением химического равновесия в результате этого воздействия: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
Запишите в таблицу выбранные цифры под соответствующими буквами.
В реактор постоянного объёма поместили оксид серы(IV) и кислород. В результате протекания обратимой реакции
2SO2(г) + О2(г) ⇄ 2SO3(г)
в реакционной системе установилось химическое равновесие.
Используя данные, приведённые в таблице, определите равновесную концентрацию SO2 (X) и исходную концентрацию O2 (Y).

Выберите из списка номера правильных ответов.
1) 0,1 моль/л
2) 0,2 моль/л
3) 0,3 моль/л
4) 0,4 моль/л
5) 0,5 моль/л
6) 0,6 моль/л
Запишите в таблицу номера выбранных веществ под соответствующими буквами.

