Химия ЕГЭ - банк заданий - страница 125
Вопросы
Нитрат хрома(III) прокалили. Образовавшееся при этом твёрдое вещество нагрели с хлоратом натрия и гидроксидом натрия. Одно из полученных веществ прореагировало с концентрированным раствором хлороводородной кислоты. Образовавшуюся при этом соль хрома выделили, растворили в воде и полученный раствор прилили к раствору карбоната натрия. Напишите уравнения четырёх описанных реакций.
Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
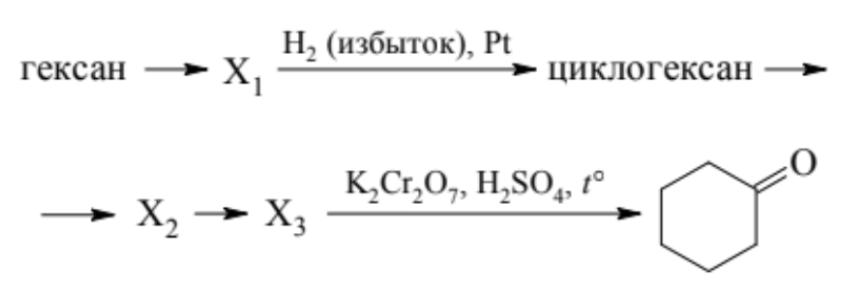
При написании уравнений реакций указывайте преимущественно образующиеся продукты, используйте структурные формулы органических веществ.
Смесь цинка и карбоната цинка, в которой соотношение числа атомов цинка к числу атомов кислорода равно 5 : 6, растворили в 500 г. разбавленного раствора серной кислоты. При этом все исходные вещества прореагировали полностью, и выделилось 22,4 л. смеси газов (н. у.). К этому раствору добавили 500 г. 40%-ного раствора гидроксида натрия. Вычислите массовую долю сульфата натрия в конечном растворе.
В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения искомых физических величин).
При сгорании 9,0 г. органического вещества А получили 15,68 л. углекислого газа (н. у.) и 5,4 г. воды.
Известно, что вещество А не содержит атомов углерода в sp3-гибридизации, а при его окислении сернокислым раствором перманганата калия образуется только одно органическое соединение — бензойная кислота.
На основании данных условия задачи:
1) проведите необходимые вычисления (указывайте единицы измерения искомых физических величин) и установите молекулярную формулу вещества А;
2) составьте структурную формулу вещества А, которая однозначно отражает порядок связи атомов в его молекуле;
3) напишите уравнение окисления вещества А раствором перманганата калия в присутствии серной кислоты (используйте структурные формулы органических веществ).
Для выполнения заданий 29, 30 используйте следующий перечень веществ:
перманганат калия, гидрокарбонат натрия, сульфит натрия, сульфат бария, гидроксид калия, пероксид водорода. Допустимо использование воды в качестве среды протекания реакции.
29. Из предложенного перечня выберите вещества, между которыми окислительно-восстановительная реакция протекает с изменением цвета раствора. Выделение осадка или газа в ходе этой реакции не наблюдается.
В ответе запишите уравнение только одной из возможных окислительно-восстановительных реакций с участием выбранных веществ. Составьте электронный баланс, укажите окислитель и восстановитель.
Из предложенного перечня выберите кислую соль и вещество, которое вступает с этой кислой солью в реакцию ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения реакции с участием выбранных веществ.
Смесь кальция и карбоната кальция, в которой массовая доля атомов кальция составляет 50%, растворили в 300 г. соляной кислоты, взятой в избытке. При этом образовался раствор массой 330 г. Один из выделившихся газов был поглощён 400 г. 4%-ного раствора гидроксида натрия. Вычислите массовую долю соли в образовавшемся после поглощения газа растворе.
В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения и обозначения искомых физических величин).
При сгорании органического вещества А массой 3,4 г. получено 4,48 л. (н. у.) углекислого газа и 1,8 г. воды. Известно, что вещество А вступает в реакцию с раствором гидроксида лития при нагревании, в результате чего образуется предельный одноатомный спирт и соль, кислотный остаток которой содержит семь атомов углерода.
На основании данных условия задачи:
1) проведите необходимые вычисления (указывайте единицы измерения и обозначения искомых физических величин) и установите молекулярную формулу вещества А;
2) составьте возможную структурную формулу вещества А, которая
однозначно отражает порядок связи атомов в его молекуле;
3) напишите уравнение реакции вещества А с раствором гидроксида лития при нагревании (используйте структурные формулы органических веществ).
При электролизе водного раствора нитрата меди(II) получили металл. Металл обработали концентрированной серной кислотой при нагревании. Выделившийся в результате газ прореагировал с сероводородом с образованием простого вещества. Это вещество нагрели с концентрированным раствором гидроксида калия. Напишите молекулярные уравнения четырёх описанных реакций.
Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения: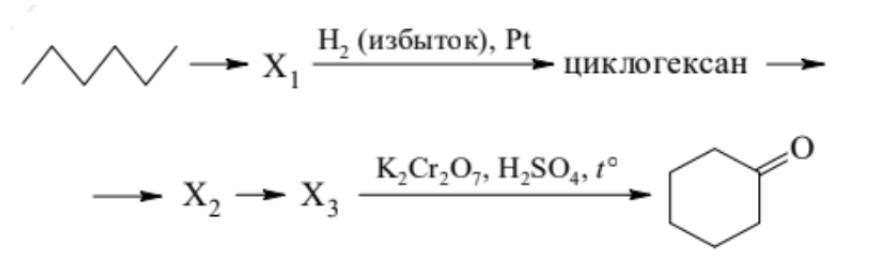
При написании уравнений реакций указывайте преимущественно образующиеся продукты, используйте структурные формулы органических веществ.
